¿Qué es LMC?
Es un tipo de cáncer en la sangre que se inicia en las células madre que se ubican en la médula ósea, el tejido esponjoso ubicado dentro de los huesos donde se producen células sanguíneas. El término crónica indica que suele progresar de manera más lenta que las formas agudas y el término mieloide hace referencia al tipo de célula afectada1.
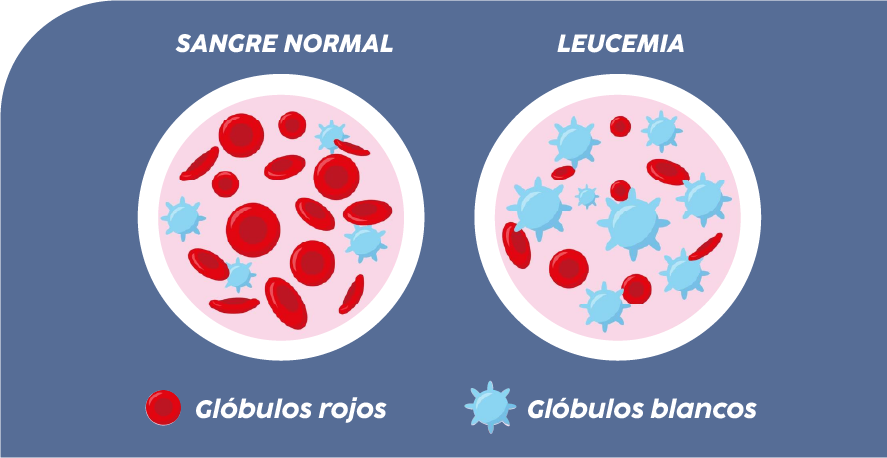
Normalmente las células de la médula ósea producen células inmaduras que se van especializando en glóbulos rojos, glóbulos blancos y/o plaquetas. La LMC se caracteriza por una sobreproducción de glóbulos blancos que se acumulan en la médula ósea y en la sangre1.
Es importante resaltar que la LMC se clasifica como neoplasia mieloproliferativa crónica (NMP) según la OMS, específicamente como “cromosoma Filadelfia positivo” debido al intercambio anormal entre parte del cromosoma 9 y parte del cromosoma 22 generando un cromosoma anormal. Esta anomalía cromosómica conduce a la producción de la proteína BCR::ABL1 aberrante, la cual es clave en la patología y en cómo respondemos al tratamiento1.
Estadística y prevalencia de la LMC
La LMC representa aproximadamente el 15% de todos los nuevos casos de leucemia en adultos2. Se ha estimado una incidencia anual de 1-1,5 casos entre 100.000 habitantes y una prevalencia alrededor de 1 entre 17.0003. En Colombia las muertes por LMC aumentaron de 130 en 2005 a 153 en 2019, con una edad media de fallecimiento que subió de 57 a 62 años4.
Entender estas estadísticas sobre la LMC nos ayuda a ser más conscientes de esta enfermedad y de su impacto tanto a nivel global como en nuestro país. Si estás enfrentando esta batalla o conoces a alguien que lo esté haciendo, recuerda que no estás solo. La información es una herramienta poderosa, mantenerse informado y consultar con profesionales de la salud es el primer paso para cuidar de ti y de tus seres queridos.


Referencias
1.Mayo Clinic. Chronic myelogenous leukemia: symptoms and causes [Internet]. Estados Unidos: Mayo Clinic; [actualizado en junio de 2021; consultado en junio de 2023]. Disponible en: https://www.mayoclinic.org/diseases-conditions/chronic-myelogenous-leukemia/symptoms-causes/syc-20352417
2.Lin Q, Mao L, Shao L, Zhu L, Han Q, Zhu H, Jin J, You L. Global, Regional, and National Burden of Chronic Myeloid Leukemia, 1990-2017: A Systematic Analysis for the Global Burden of Disease Study 2017. Front Oncol [Internet]. 2020 [consultado en diciembre de 2023];10. Disponible en: https://www.frontiersin.org/journals/oncology/articles/ 10.3389/fonc.2020.580759/full
3.Instituto de Evaluación Tecnológica en Salud IETS. Posicionamiento terapéutico para el tratamiento farmacológico de la leucemia mieloide crónica con inhibidores de la tirosina quinasa. Bogotá D.C.: Instituto de Evaluación Tecnológica en Salud IETS y Ministerio de Salud y Protección Social; 2021.
4.Instituto de Evaluación Tecnológica en Salud IETS. Posicionamiento terapéutico para el tratamiento farmacológico de la leucemia mieloide crónica con inhibidores de la tirosina quinasa. Bogotá D.C.: Instituto de Evaluación Tecnológica en Salud IETS y Ministerio de Salud y Protección Social; 2021.
Novartis de Colombia S.A. Calle 93B No. 16-31. PBX 654 44 44. Bogotá, D.C. Novartis Pharma, AG de Basilea, Suiza. ® = Marca registrada. Material dirigido a público general. Más información en el Departamento Médico de Novartis S.A Colombia: 6544444 o al correo electrónico: [email protected]. Si desea reportar un evento adverso ingrese al siguiente link: https://www.report.novartis.com/es o a través del correo electrónico: [email protected]. Este material no es promocional en lenguaje, apariencia o intención. Si se hace alusión a productos o indicaciones no aprobados por la autoridad regulatoria del país, será bajo el estricto propósito educativo, de genuino intercambio científico y para incluir las alternativas de tratamiento de forma balanceada, completa y vigente. Este material no pretende sustituir o reemplazar una decisión clínica ni terapéutica. No se autoriza la grabación, toma de fotografías y distribución del material y tampoco difusión por medios no autorizados por Novartis. Fecha de aprobación: 17/09/2024 Fecha de caducidad: 17/09/2026 ID de Código de aprobación: FA-11273216